
2025年5月7日,创新双特异性抗体高罗华(格菲妥单抗)新适应症在华获批,联合吉西他滨与奥沙利铂(GemOx)用于治疗不适合自体造血干细胞移植(ASCT)的复发或难治性弥漫大B细胞淋巴瘤非特指型(DLBCL NOS)成人患者[1]。同年12月7日,该药成功列入2025年国家医保药品目录,成为唯一纳入国家医保的T细胞免疫疗法,价格大幅降低并于2026年1月1日正式执行,标志着我国淋巴瘤治疗在疗效与可及性上同步迈入“双抗”新时代[2][3]。本文将深入解析格菲妥单抗如何以其独特机制、显著的生存获益、可控的安全性以及全新的医保支付方案,为不适合移植的复发/难治性弥漫大B细胞淋巴瘤(R/R DLBCL)患者提供关键的破局之道。
DLBCL越复发越难治,如果二线治疗无法达到缓解,后续治疗选择将越来越少。因此,找到有效且安全的二线疗法改善患者预后,在更早阶段抓住控制疾病的契机,是提高DLBCL生存率的关键一环[4]。近年来,T细胞免疫疗法飞速发展,正在引领着DLBCL二线和后线治疗的全面革新。其中,CAR-T由于制备期长,管理程序冗长复杂,加之可及性等问题,其在临床中的应用范围仍有较大限制。如今,作为‘即用型’T细胞疗法的双抗药物,临床适应症应用范围拓宽,为DLBCL二线治疗带来了全新解题思路[4]。
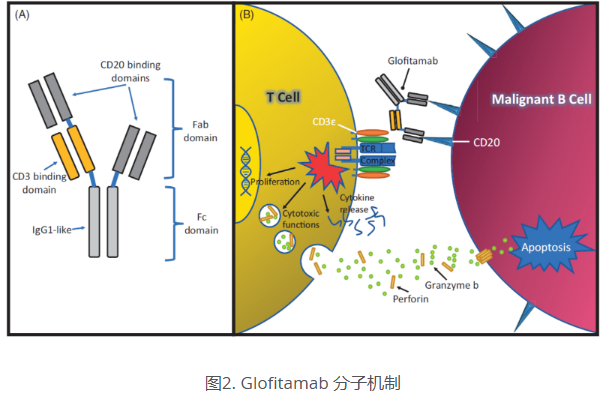
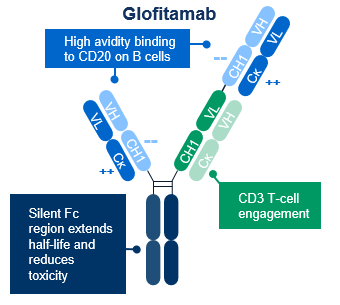
格菲妥单抗是一种创新的双特异性抗体,其核心优势在于其“即用型”特性与独特的作用机制。它依托新型的2:1双抗结构,可同时靶向结合T细胞表面的CD3抗原和B细胞表面的CD20抗原,从而激活、扩增并重定向T细胞,带来更强的B细胞抓取能力和作用效力,在安全耐受的前提下加强杀伤肿瘤细胞的能力[5][6]。具体而言,其CD20结合结构域来源于高亲和力的Type II CD20抗体奥妥珠单抗,可二价结合B细胞上的CD20;而T细胞结合域则以单价形式识别CD3ε链,激活T细胞不受TCR特异性或MHC限制[7]。通过与B细胞上的CD20和T细胞上的CD3同时结合,格菲妥单抗介导免疫突触形成,进而引发强效的T细胞活化、增殖、细胞因子分泌和细胞溶解蛋白释放,最终导致表达CD20的B细胞被溶解[8]。这一机制有助于患者获得早期、深度的缓解,降低疾病进展风险[5]。
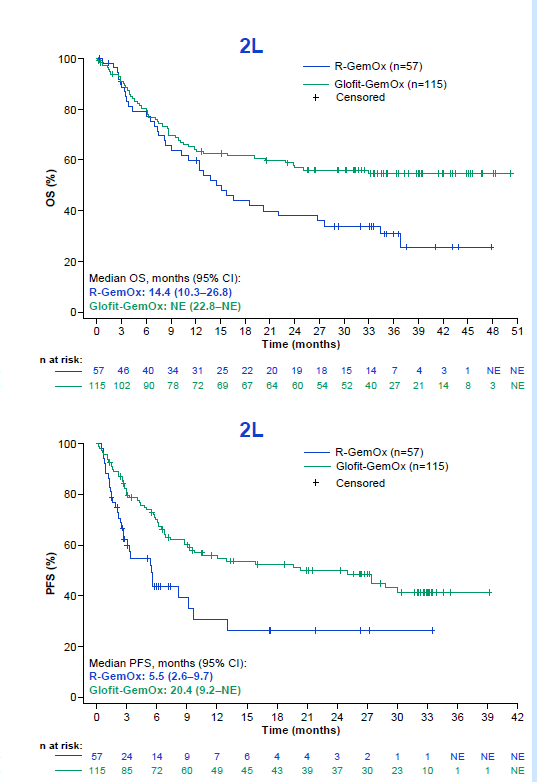
格菲妥单抗联合吉西他滨与奥沙利铂(Glofit-GemOx)方案为不适合移植的R/R DLBCL患者带来了前所未有的长期生存改善。根据全球III期STARGLO研究的3年随访数据,该方案相较于传统利妥昔单抗联合GemOx(R-GemOx)方案,展现出全面且持续的疗效优势[9][10]。
在既往仅接受过一线治疗的患者中,Glofit-GemOx组的临床获益尤为显著:其3年总生存(OS)率高达55%,中位OS未达到(对照组为14.4个月),死亡风险降低42%(HR=0.58);中位无进展生存(PFS)达到20.4个月,是对照组5.5个月的近四倍,疾病进展或死亡风险降低51%(HR=0.49);完全缓解(CR)率提升至63.5%,显著优于对照组的28.1%[9][10]。华中科技大学血液病学研究所所长胡豫教授指出:“根据STARGLO研究结果,接受高罗华联合治疗的患者,中位总生存期几乎可以实现翻倍,中位OS达25.5个月(R-GemOx组12.9个月);其中位无进展生存期翻近四倍(13.8个月 VS. 3.6个月),总缓解率和完全缓解率相比于对照组分别提高 27.7% 和 33.2%。”[11]
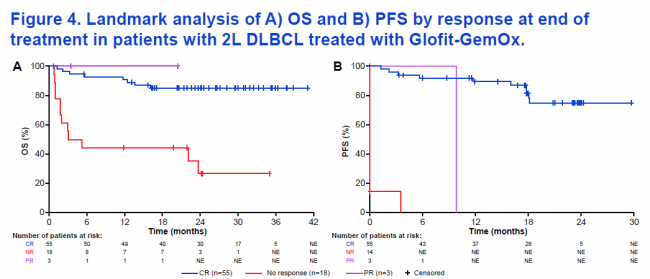
亚组分析进一步证实,无论患者属于难治或早期复发(一线治疗后≤12个月),还是晚期复发(>12个月),Glofit-GemOx方案均能带来更高的生存率和缓解率[9][10]。更令人鼓舞的是,对于治疗结束时达到CR的患者,其治疗后24个月的OS率和PFS率分别高达85.2%和74.8%,意味着深度缓解能够转化为持久的生存获益[10]。胡豫教授补充道:“长远来看,高罗华采用12周期的固定疗程,可以减少患者就诊的次数、往返医院和住所所需的成本和时间等,有望帮助节省后线治疗医疗资源。”[12]
格菲妥单抗在二线治疗R/R DLBCL中展现出了与CAR-T疗法相当的长期疗效,且在无进展生存期和安全性管理上可能更具优势。STARGLO研究的3年OS率(55%)与ZUMA-7研究中CAR-T疗法(阿基仑赛)的4年OS率(54.6%)相当,其中位PFS(20.4个月)甚至优于阿基仑赛的14.7个月,CR率(63.5%)亦与后者的65%接近[13]。
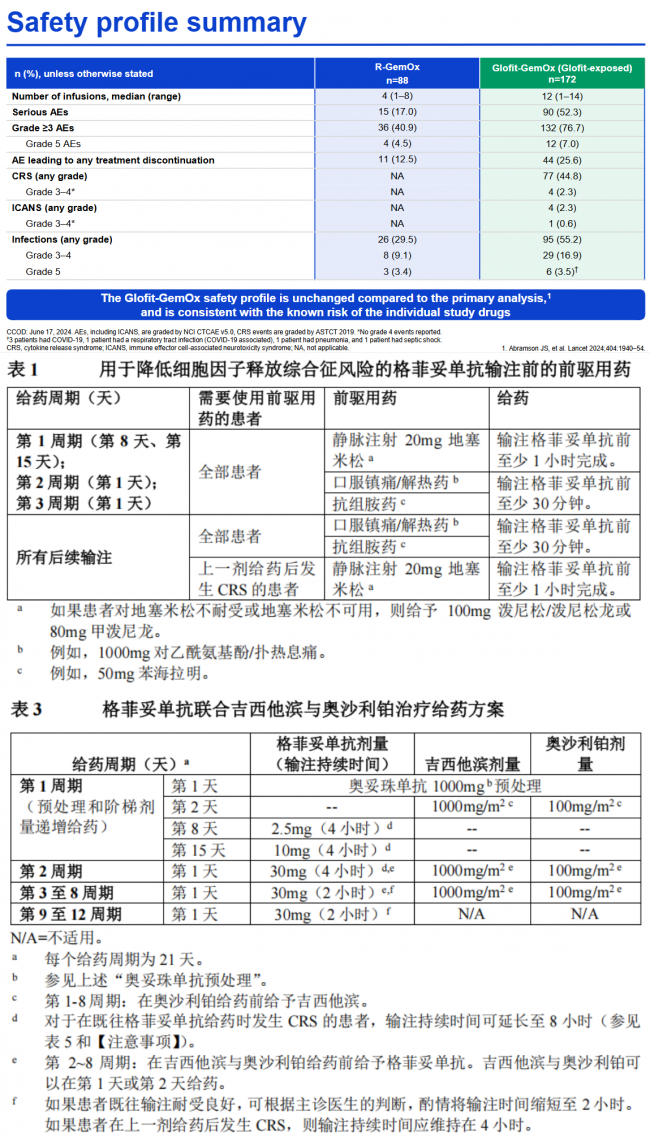
在安全性方面,格菲妥单抗显示出更可控的细胞因子释放综合征(CRS)风险。STARGLO研究中,所有等级CRS发生率为44.8%,且绝大多数为1-2级,≥3级CRS发生率仅为2.3%;免疫效应细胞相关神经毒性综合征(ICANS)发生率仅2.3%[14]。相比之下,ZUMA-7研究中CAR-T疗法的所有等级CRS发生率高达92%,≥3级为6%;所有等级神经毒性发生率达60%[14]。格菲妥单抗通过奥妥珠单抗预处理和阶梯剂量递增给药方案,有效降低了CRS的风险[14]。其在中国患者中的安全性特征与全球数据一致,总体获益-风险比良好,且药物相互作用影响小,老年人及轻中度肝肾功能不全患者均可使用[15]。
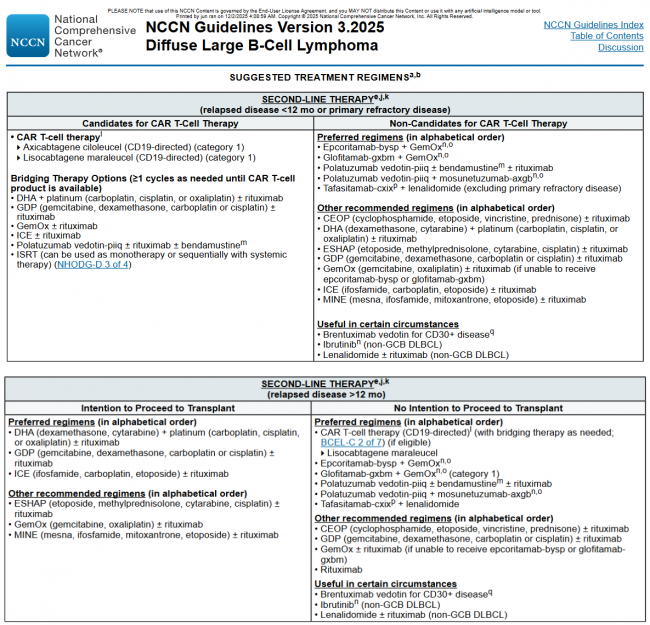
格菲妥单抗已获得国内外多部权威指南的高级别推荐,确立了其在R/R DLBCL治疗标准中的核心地位。最新版NCCN指南(2025 V3)推荐,对于首次复发>12个月且不适合移植的DLBCL患者,优选格菲妥单抗联合GemOx方案(1类推荐)[16]。同时,《细胞免疫疗法治疗侵袭性B细胞淋巴瘤中国专家共识(2025)》将格菲妥单抗与CAR-T同归类为T细胞疗法并予以推荐;《中国肿瘤整合诊治指南(CACA)淋巴瘤(2024)》也推荐其用于不适合移植的R/R DLBCL患者;《ESMO-EHA淋巴瘤指南(2025年版)》同样给予格菲妥单抗联合GemOx方案1A级推荐[17]。
格菲妥单抗纳入2025年国家医保药品目录,是其提升临床可及性的里程碑事件,从根本上减轻了患者的经济负担。2025年12月7日,新版国家医保目录发布,格菲妥单抗作为谈判成功的创新药之一被纳入[2][3]。湖南省肿瘤医院副院长周辉指出:“纳入医保目录后,自2026年1月1日起,该药品价格大幅度下降的同时,还可纳入医保报销,患者自付金额将明显下降,对这类患者来说是一个非常利好的消息。”[3] 国谈前该药价格为12650元/支,需患者全自费,医保覆盖后患者自付费用将显著降低[3]。本次纳入医保支付范围覆盖了其全部已获批适应症:单药用于至少两线治疗后的R/R DLBCL,以及联合GemOx用于不适合移植的R/R DLBCL NOS患者[5]。
对于不适合移植的R/R DLBCL患者,格菲妥单抗联合GemOx是一个明确且有效的治疗选择。以一个典型病例为例:患者为77岁男性,确诊CD20阳性DLBCL,一线R-CHOP化疗后12个月内早期复发。因高龄不适合自体干细胞移植(ASCT),且未接受过CAR-T或双抗治疗[18]。根据其病情(复发/难治、不适合ASCT)和病理类型(需确认为DLBCL NOS),该患者可选择格菲妥单抗联合GemOx方案[19]。
其标准给药方案为:第1周期第1天完成奥妥珠单抗预处理后,在第8天和第15天分别阶梯式给予格菲妥单抗2.5mg和10mg;第2-8周期,每周期第1天给予格菲妥单抗30mg,并联合吉西他滨与奥沙利铂化疗;第9-12周期,继续每周期第1天给予格菲妥单抗30mg进行单药巩固治疗[20]。通过规范的阶梯剂量递增和预处理,可有效管理CRS等风险,使患者完成固定周期治疗,追求深度持久缓解[14]。
格菲妥单抗(高罗华)新适应症的获批与国家医保的覆盖,共同构建了R/R DLBCL二线治疗的新范式。其基于2:1双抗结构的“即用型”T细胞重定向杀伤机制,通过固定周期的Glofit-GemOx方案,为不适合移植的患者带来了显著的生存延长与深度缓解,疗效媲美甚至部分优于CAR-T,且安全性更易管理。随着其被写入国内外多项权威指南并大幅降价纳入医保,这一创新疗法已从临床证据扎实的“优势选择”,转变为可及性高的“标准方案”,真正让更多中国DLBCL患者有机会在更早的治疗阶段获得生存突破,重燃治疗希望。
参考文献
1. 罗氏制药中国. 创新双特异性抗体高罗华新适应症在华获批.. https://www.medsci.cn/article/show_article.do?id=0d8b8e5128c2
2. 《2025年国家基本医疗保险、生育保险和工伤保险药品目录》.
3. 新版国家医保药品目录及首版商保创新药目录正式发布.
4. 哈尔滨血液病肿瘤研究所所长马军教授观点,https://www.toutiao.com/article/7501912661454488116/Bacac M, Colombetti S, Herter S, et al. CD20-TCB with Obinutuzumab Pretreatment as Next-Generation Treatment of Hematologic Malignancies. Clin Cancer Res. 2018 Oct 1;24(19):4785-4797.
5. 华中科技大学血液病学研究所所长胡豫教授指出,“作为一类无需定制化的即用型T细胞疗法...”,https://www.toutiao.com/article/7501912661454488116/?&source=m_redirect&wid=1766484864151
6. Martin Hutchings, C.C.-S., Emmanuel Bach, et al. 403 Glofitamab Step-up Dosing Induces High Response Rates in Patients with Hard-to-Treat Refractory or Relapsed Non-Hodgkin Lymphoma. ASH 2020.
7. 格菲妥单抗注射液说明书(2025年9月30日)适应症部分.
8. Jeremy Abramson, et al. Sustained clinical benefit of glofitamab plus gemcitabine and oxaliplatin (GemOx) versus rituximab plus GemOx (R-GemOx) in patients with relapsed/refractory (R/R) diffuse large B-cell lymphoma (DLBCL): 3-year follow-up of STARGLO . 2025 ASH. Poster 5519.
9. Haifaa Abdulhaq, et al. Glofitamab plus gemcitabine and oxaliplatin (GemOx) vs rituximab (R)-GemOx in patients with relapsed/refractory (R/R) diffuse large B-cell lymphoma (DLBCL): efficacy and safety in patient subgroups. 2025 ASH P3743.
10. 华中科技大学血液病学研究所所长胡豫教授指出,“根据STARGLO研究结果...”,http://m.toutiao.com/group/7501912661454488116/
11. 华中科技大学血液病学研究所所长胡豫教授观点,https://www.toutiao.com/article/7501912661454488116/?&source=m_redirect&wid=1766484864151
12. Westin JR, et al. N Engl J Med. 2023 Jul 13;389(2):148-157.
13. Jeremy S Abramson, Matthew Ku, Mark Hertzberg, et al. Glofitamab plus gemcitabine and oxaliplatin (GemOx) versus rituximab-GemOx for relapsed or refractory diffuse large B-cell lymphoma (STARGLO): a global phase 3, randomised, open-label trial. Lancet. 2024 Nov 16;404(10466):1940-1954.
14. 格菲妥单抗注射液说明书(2025年9月30日)安全性部分.
15. NCCN B细胞淋巴瘤指南(2025V3).
16. 细胞免疫疗法治疗侵袭性B细胞淋巴瘤中国专家共识(2025);《中国肿瘤整合诊治指南(CACA) 淋巴瘤(2024)》;《ESMO-EHA淋巴瘤指南(2025年版)》.
17. 典型病例描述.
18. 格菲妥单抗注射液说明书(2025年9月30日)作用机制部分.
19. 格菲妥单抗注射液说明书(2025年9月30日)用法用量部分.
20. Locke FL, et al. N Engl J Med. 2022 Feb 17;386(7):640-654.
21. CAR T细胞治疗NHL毒副作用临床管理专家共识[J].转化医学杂志,2021,10(01):1-11.
22. 2025年CSCO淋巴瘤诊疗指南.
